1)克隆PCR产物的最优条件是什么?
最佳插入片段:载体比需实验确定。1:1(
插入片段:载体)常为最佳比,摩尔数比1:8或8:1也行。应测定比值范围。连接用5ul 2X连接液,50ng
质粒DNA,1Weiss单位的T4
连接酶,
插入片段共10ul。室温保温1小时,或4℃过夜。在这2种温度下,缺T-凸出端的载体会自连,产生蓝斑。室温保温1小时能满足大多数克隆要求,为提高连接效率,需4℃过夜。
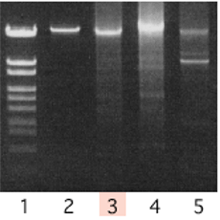
2)PCR产物是否需要用凝胶纯化?
如凝胶分析扩增产物只有一条带,不需要用凝胶纯化。如可见其他杂带,可能是积累了大量引物的二聚体。少量的引物二聚体的
摩尔数也很高,这会产生高比例的带有引物二聚体的克隆,而非目的
插入片段。为此需在克隆前做凝胶纯化。
3)如果没有回收到目的片段,还需要作什么对照实验?
A)涂布未转化的感受态细胞。
如有菌落,表明氨苄失效,或污染上带有氨苄抗型的质粒,或产生氨苄抗型的菌落。
B)转化完整质粒,计算菌落生长数,测定转化效率。
例如,将1ug/ul质粒1:100稀释,1ul用于100ul感受态细胞转化。用SOC稀释到1000ul后,用100ul铺板。培养过夜,产生1000个菌落。转化率为:产生菌落的总数/铺板DNA的总量。
铺板DNA的总量是转化反应所用的量除以稀释倍数。具体而言转化用10ng DNA,用SOC稀释到1000u后含10 ng DNA,用1/10铺板,共用1 ng DNA。转化率为:
1000克隆X10
3 ng /铺板1 ng DNA ug=10
6cfu/ ug
转化pGEM-T应用10
8cfu/ ug感受态细胞
如没有菌落或少有菌落,感受态细胞的转化率太低。
C)如用pGEM-T正对照,或PCR产物,产生>20-40蓝斑(用指定步骤10
8cfu/ug感受态细胞),表明载体失去T。可能是连接酶污染了
核酸酶。T4
DNA连接酶(M1801,M1804,M1794)质量标准好无核酸酶污染,不应用其它来源的T4 DNA连接酶替换。
D)用pGEM-T或pGEM-T Easy载体,连接pGEM-T正对照,转化高频率感受态细胞(10
8cfu/ug),按照指定的实验步骤,可得100个菌落,其中60%应为白斑,如产生>20-40蓝斑,没有菌落或少有菌落,连接有问题。
4)对照实验结果好,却没有回收到目的片段,实验出了什么问题?
A)连接用室温保温1小时,能满足大多数克隆,为提高效率,需4℃过夜。
B)插入片段带有污染,使3`-T缺失,或抑制连接,抑制转化。为此,将
插入片段和pGEM-T正对照混合,再连接。如降低了对照的菌落数,
插入片段需纯化,或重新制备。如产生大量的蓝斑,
插入片段污染有核酸酶,使pGEM-T或pGEM-T Easy载体3`-T缺失。
C)插入片段不适于连接。用凝胶纯化的
插入片段,因受UV过度照射,时有发生。UV过度照射会产生
嘧啶二聚体,不利于连接,DNA必需重新纯化。
D)带有修复功能的耐热DNA聚合酶的扩增产物末端无A,后者是pGEM-T或pGEM-T Easy载体克隆所需。加Taq DNA聚合酶和
核苷酸可在末端加A。详情查pGEM-T pGEM-T Easy载体技术资料(TM042)。
E)
高度重复序列可能会不稳定,在扩增中产生缺失和重排,如发现插入片段高频率地产生缺失和重排,需用重组缺陷大肠杆菌菌株,如SURE细胞
PCR反应体系与反应条件
标准的PCR反应体系:
10×扩增缓冲液 10ul
4种dNTP混合物 各200umol/L
引物 各10~100pmol
模板DNA 0.1~2ug
Taq DNA聚合酶 2.5u
Mg2+ 1.5mmol/L
加双或三蒸水至 100ul
PCR反应五要素:参加PCR反应的物质主要有五种即引物、酶、dNTP、模板和Mg2+
引物:引物是PCR特异性反应的关键,PCR 产物的特异性取决于引物与模板DNA互补的程度。理论上,只要知道任何一段模板DNA序列, 就能按其设计互补的寡核苷酸链做引物,利用PCR就可将模板DNA在体外大量扩增。
原则:
①引物长度:15-30bp,常用为20bp左右。
②引物扩增跨度:以200-500bp为宜,特定条件下可扩增长至10kb的片段。
③引物碱基:参照引物设计的基本原则
④避免引物内部出现二级结构,避免两条引物间互补,特别是3'端的互补,否则会形成引物二聚体,产生非特异的扩增条带。
⑤引物3'端的碱基,特别是最末及倒数第二个碱基,应严格要求配对,以避免因末端碱基不配对而导致PCR失败。
⑥引物中有或能加上合适的酶切位点, 被扩增的靶序列最好有适宜的酶切位点, 这对酶切分析或分子克隆很有好处。
⑦引物的特异性:引物应与核酸序列数据库的其它序列无明显同源性。引物量:每条引物的浓度0.1~1umol或10~100pmol,以最低引物量产生所需要的结果为好,引物浓度偏高会引起
错配和非特异性扩增,且可增加引物之间形成
二聚体的机会。
酶及其浓度
目前有两种Taq DNA聚合酶供应, 一种是从栖热水生杆菌中提纯的天然酶,另一种为大肠菌合成的基因工程酶。催化一典型的PCR反应约需酶量2.5U(指总反应体积为100ul时),浓度过高可引起非特异性扩增,浓度过低则合成产物量减少。
dNTP的质量与浓度
dNTP的质量与浓度和PCR扩增效率有密切关系,dNTP粉呈颗粒状,如保存不当易变性失去生物学活性。dNTP溶液呈酸性,使用时应配成高浓度后,以1M NaOH或1M Tris。HCL的缓冲液将其PH调节到7.0~7.5,小量分装,-20℃冰冻保存。多次冻融会使dNTP降解。在PCR反应中,dNTP应为50~200umol/L,尤其是注意4种dNTP的浓度要相等(等摩尔配制),如其中任何一种浓度不同于其它几种时(偏高或偏低),就会引起
错配。浓度过低又会降低PCR产物的产量。dNTP能与Mg2+结合,使游离的Mg2+浓度降低。
模板(靶基因)核酸 模板核酸的量与纯化程度,是PCR成败与否的关键环节之一,传统的DNA纯化方法通常采用SDS和蛋白酶K来消化处理标本。SDS的主要功能是:溶解细胞膜上的脂类与蛋白质,因而溶解膜蛋白而破坏细胞膜,并解离细胞中的核蛋白,SDS还能与蛋白质结合而沉淀;蛋白酶K能水解消化蛋白质,特别是与DNA结合的
组蛋白,再用有机溶剂酚与氯仿抽提掉蛋白质和其它
细胞组份,用乙醇或
异丙醇沉淀核酸。提取的核酸即可作为模板用于PCR反应。一般临床检测标本,可采用快速简便的方法溶解细胞,裂解病原体,消化除去染色体的蛋白质使靶基因游离,直接用于PCR扩增。RNA模板提取一般采用
异硫氰酸胍或蛋白酶K法,要防止RNase降解RNA。
dntp
Mg2+浓度 Mg2+对PCR扩增的特异性和产量有显著的影响,在一般的PCR反应中,各种dNTP浓度为200umol/L时,Mg2+浓度为1.5~2.0mmol/L为宜。Mg2+浓度过高,反应
特异性降低,出现非特异扩增,浓度过低会降低Taq DNA聚合酶的活性,使反应产物减少。
PCR反应条件的选择
PCR反应条件为温度、时间和循环次数。
温度与时间的设置:基于PCR原理三步骤而设置变性-退火-延伸三个温度点。在标准反应中采用三温度点法,双链DNA在90~95℃变性,再迅速冷却至40~60℃,引物退火并结合到靶序列上,然后快速升温至70~75℃,在Taq DNA聚合酶的作用下,使引物链沿模板延伸。对于较短靶基因(长度为100~300bp时)可采用二温度点法,除变性温度外、退火与延伸温度可合二为一,一般采用94℃变性,65℃左右退火与延伸(此温度Taq DNA酶仍有较高的
催化活性)。
①变性温度与时间:变性温度低,解链不完全是导致PCR失败的最主要原因。一般情况下,93℃~94℃min足以使模板DNA变性,若低于93℃则需延长时间,但温度不能过高,因为高温环境对酶的活性有影响。此步若不能使靶基因模板或PCR产物完全变性,就会导致PCR失败。
②退火(复性)温度与时间:退火温度是影响PCR特异性的较重要因素。变性后温度快速冷却至40℃~60℃,可使引物和模板发生结合。由于模板DNA比引物复杂得多,引物和模板之间的碰撞结合机会远远高于模板
互补链之间的碰撞。
退火温度与时间,取决于引物的长度、
碱基组成及其浓度,还有靶基序列的长度。对于20个核苷酸,G+C含量约50%的引物,55℃为选择最适
退火温度的起点较为理想。引物的
复性温度可通过以下公式帮助选择合适的温度:
Tm值(解链温度)=4(G+C)+2(A+T)
复性温度=Tm值-(5~10℃)
在Tm值允许范围内, 选择较高的复性温度可大大减少引物和模板间的非特异性结合, 提高PCR反应的特异性。复性时间一般为30~60sec,足以使引物与模板之间完全结合。
③延伸温度与时间:Taq DNA聚合酶的生物学活性:
70~80℃ 150核苷酸/S/酶分子
70℃ 60核苷酸/S/酶分子
55℃ 24核苷酸/S/酶分子
高于90℃时, DNA合成几乎不能进行。
PCR反应的延伸温度一般选择在70~75℃之间,常用温度为72℃,过高的延伸温度不利于引物和模板的结合。PCR延伸反应的时间,可根据待扩增片段的长度而定,一般1Kb以内的DNA片段,延伸时间1min是足够的。3~4kb的靶序列需3~4min;扩增10Kb需延伸至15min。延伸进间过长会导致非特异性扩增带的出现。对低浓度模板的扩增,延伸时间要稍长些。
实验室布局
PCR实验室按规定需要四间,分别是1 试剂储存和准备区、2 标本制备区、3扩增反应混合物配制和扩增区、4扩增产物分析区,布局见图1。

pcr实验室
图1 四间PCR实验室区域设置
如果使用全自动分析仪,各区域可适当合并,我们建议将扩增区和产物分析区合并为扩增检测区即共三个间,布局见图2。
图2 三间PCR实验室区域设置
按国家卫生部的要求,进入各个工作区域必须严格遵循单一方向顺序,即只能从试剂储存和准备区?标本制备区扩增反应混合物配制和扩增区?扩增产物分析区,避免发生交叉污染。各工作区必须安装适当的排风设备确保空气流向按单一方向。工作区的墙面、地面、办公用品等必须选用耐消毒药品腐蚀的材料。工作区必须有明确的标记,避免不同工作区域内的设备、物品混用。
设置标准
各工作区域必须配备排风扇、空调、耐腐蚀地面和工作台面、更衣柜、鞋柜、专用办公用品、专用工作服和工作鞋、移动紫外灯等,保证安全卫生需要。
根据国家卫生部《临床基因扩增检验实验室基本设置标准》,各工作区域必备仪器设备如下:
一 试剂储存和准备区
1.2-8℃和-15℃冰箱
2.混匀器
3.微量加样器(覆盖1-1000μl)
4.移动紫外灯(近工作台面)
5.消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头(带滤心)
6.专用工作服和工作鞋
7.专用办公用品
二标本制备区
1.2-8℃冰箱、-20℃或-80℃冰箱
2.高速台式冷冻离心机
3.混允器
4.水浴箱或加热模块
5.微量加样器(覆盖1-1000μl)
6.可移动紫外灯(近工作台面)
7.超净工作台
8.消耗品:与“试剂储存与准备区”的消耗品相同
9.专用工作服和工作鞋
10.专用办公用品
如需处理大分子DNA,应具有超声波水浴仪。
三基因扩增区和产物分析区
1. 全自动定量核酸扩增仪(含计算机、打印机)
2. 微量加样器(覆盖1-1000μl)
3. 可移动紫外灯(近工作台面)
4. 消耗品:与“试剂储存与准备区”的消耗品相同
5. 专用工作服和工作鞋
6. 专用办公用品
各工作区域必须有明确的标记,避免不同工作区域内的设备、物品混用。在不同的工作区域应使用不同颜色或有明显区别标志的工作服,以便于鉴别。当工作者离开工作区时,不得将各区特定的工作服带出。
3.实验室质量管理
PCR实验室内工作人员必须参加由国家卫生部或各省临床检验中心举办的临床
基因扩增培训班,并持证上岗。PCR实验室通过验收,实验室至少必须应有两个以上持有“临床基因检测上岗证”。PCR实验室必须建立严格的实验室
管理制度、建立标准化操作程序(SOP)、建立系列质量管理文件等,确保实验室日常运行符合国家卫生部的要求,确保检测结果准确、确保实验室卫生安全,确保实验室长期稳定运行。
各种变体
1.
递减PCR(touchdown PCR):前几循环温度逐渐下降。
3.热启动PCR(hot start PCR):以高热活化型核酸聚合酶进行反应,减少非专一性产物。
4.即时PCR(real-time PCR):PCR过程中利用萤光探针或染料定量检测,又称定量PCR(quantitative PCR)。
5.
巢式PCR(nested PCR):先用低特异性引物扩增几个循环以增加模板数量,再用高特异性引物扩增。
6.
多重PCR(multiplex PCR):在同一个管中使用多组引物。
7.复原条件PCR(reconditioning PCR):PCR产物稀释10倍后重新放入原浓度的引物和dNTP等循环3次,以消除产物中的异二聚体。
8.dsRNA合成(dsRNA replicator):合并使用high-fidelity DNA polymersae、
T7RNA聚合酶与Phi6 RNA replicase;从双股DNA转录为对应的双股RNA(dsRNA)。可应用于RNAi实验操作。
9.COLD-PCR(
co-amplification at
lower
denaturation temperature-PCR):用以检测突变或特殊等位基因的PCR应用技术。