西比灵
百科内容来自于:

成份
性状
适应症
规格
用法用量
1.偏头痛的预防性治疗
- 起始剂量:对于65岁以下患者开始治疗时可给予每晚2粒,65岁以上患者每晚1粒。如在治疗中出现抑郁、锥体外系反应和其它严重的不良反应,应及时停药。如在治疗2个月后未见明显改善,则可视为病人对本品无反应,可停止用药。
- 维持治疗:如果疗效满意,患者需维持治疗时,应减至每7天连续给药5天(剂量同上)、停药2天。即使预防性维持治疗的疗效显著,且耐受性良好,在治疗6个月后也应停药观察,只有在复发时才应重新服药。
2.眩晕
每日剂量应与上相同,但应在控制症状后及时停药,初次疗程通常少于2个月。如果治疗慢性眩晕症1个月或突发性眩晕症2个月后症状未见任何改善则应视为患者对本品无反应,应停药。
- 起始剂量:对于65岁以下患者开始治疗时可给予每晚2粒,65岁以上患者每晚1粒。如在治疗中出现抑郁、锥体外系反应和其它严重的不良反应,应及时停药。如在治疗2个月后未见明显改善,则可视为病人对本品无反应,可停止用药。
- 维持治疗:如果疗效满意,患者需维持治疗时,应减至每7天连续给药5天(剂量同上)、停药2天。即使预防性维持治疗的疗效显著,且耐受性良好,在治疗6个月后也应停药观察,只有在复发时才应重新服药。
2.眩晕
每日剂量应与上相同,但应在控制症状后及时停药,初次疗程通常少于2个月。如果治疗慢性眩晕症1个月或突发性眩晕症2个月后症状未见任何改善则应视为患者对本品无反应,应停药。
不良反应
临床试验数据
安慰剂对照双盲试验数据
报告率不少于1%的不良反应
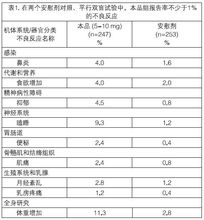
两个安慰剂对照、平行双盲临床试验评估了本品的安全性(5-10mg/日),500名受试者参与试验,其中247名患者使用本品,253名患者使用安慰剂。两个试验对受试者分别进行偏头痛和眩晕治疗。
在这些试验中,本品组报告率不少于1%的不良反应(ADR)见表1。
活性药物对照试验数据-报告率不少于1%的不良反应
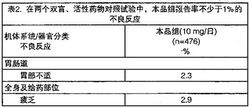
选用两个双盲活性药物对照试验来测定ADR的发生率。这两个试验对476名受试者分别进行偏头痛和眩晕/偏头痛的治疗,每日给予受试者10mg本品。
在活性药物的对照临床试验中,报告率不少于1%但未列在表1的不良反应见表2。
安慰剂和活性对照试验数据-不良反应
报告率不少于1%的不良反应
在上述两个临床试验的数据表中,报告率少于1%的其他ADR见表3。
上市后经验
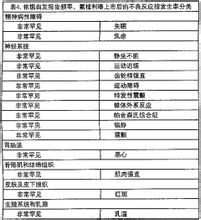
上市后首次判定为氟桂利嗪不良反应的不良事件见表4。不良反应按自发报告率分类:
很常见≥1/10
常见≥1/100,且1/10
少见≥1/1,000,且<1/100
罕见≥1/10,000,且1/1,000
非常罕见<1/10,000,包括个别病例。
依据自发报告率,以下不良反应按发生分类列于表4。
安慰剂对照双盲试验数据
报告率不少于1%的不良反应
两个安慰剂对照、平行双盲临床试验评估了本品的安全性(5-10mg/日),500名受试者参与试验,其中247名患者使用本品,253名患者使用安慰剂。两个试验对受试者分别进行偏头痛和眩晕治疗。
在这些试验中,本品组报告率不少于1%的不良反应(ADR)见表1。
活性药物对照试验数据-报告率不少于1%的不良反应
选用两个双盲活性药物对照试验来测定ADR的发生率。这两个试验对476名受试者分别进行偏头痛和眩晕/偏头痛的治疗,每日给予受试者10mg本品。
在活性药物的对照临床试验中,报告率不少于1%但未列在表1的不良反应见表2。
安慰剂和活性对照试验数据-不良反应
报告率不少于1%的不良反应
在上述两个临床试验的数据表中,报告率少于1%的其他ADR见表3。
上市后经验
上市后首次判定为氟桂利嗪不良反应的不良事件见表4。不良反应按自发报告率分类:
很常见≥1/10
常见≥1/100,且1/10
少见≥1/1,000,且<1/100
罕见≥1/10,000,且1/1,000
非常罕见<1/10,000,包括个别病例。
依据自发报告率,以下不良反应按发生分类列于表4。
禁忌
注意事项
孕妇及哺乳期妇女用药
儿童用药
老年用药
药物相互作用
药物过量
药理毒理
药理作用
盐酸氟桂利嗪为选择性钙拮抗剂,可阻滞过量的钙离子跨膜进入细胞内,防止细胞内钙负荷过量,也可防止缺血缺氧时大量钙进入神经元,改善脑微循环及神经元代谢,抑制脑血管痉挛、血小板凝聚及血液粘滞度增高等,此外还有细胞膜稳定作用。本品脂溶性高,易透过血脑屏障。
本品对心脏收缩和传导无影响。
毒理研究
本品的非临床中枢神经系统作用(如;镇静、唾液分泌和共济失调)仅当暴露量远远超过人体的最大暴露量时才观察到,与临床使用的相关性很小。
对本品的安全性进行了一系列综合的非临床研究,包括:单次口服给药的毒性(小鼠、成年及幼年大鼠、豚鼠)、腹膜内(小鼠和大鼠)、皮下(小鼠和大鼠)、静脉(小鼠和大鼠)以及动脉内(大鼠)给药;重复口服给药的毒性(犬12个月和大鼠18个月多剂量的口服毒性)、静脉毒性(犬3个月和大鼠1个月);口服给药的生殖试验测试大鼠的生育和总体繁殖能力;大鼠、兔和出生前、后大鼠的致畸性和胚胎毒性。对本品的致突变性进行了一系列广泛的研究,包括:鼠伤寒沙门氏菌的体外位点和/或基因突变试验、果蝇的伴性隐性致死试验、人体内淋巴细胞的染色体畸变试验、小鼠的体内微核和显性致死试验。利用口服给药后小鼠和大鼠模型的寿命评估本品致癌性。
单次口服给药的毒性试验(小鼠的LD 50约为960-1896mg/kg;大鼠的LD 50约为343-1935mg/kg)结果与人体的最大治疗剂量(对50kg的患者约为0.2mg/kg)相比,本品有很大的安全范围。大鼠和犬重复口服给药的毒性试验结果显示一些临床作用可能与过度的药理作用相关,但都是在远远超过药物治疗剂量时观察到的(按mg/kg计算约为人体最大治疗剂量的400倍),且与临床使用的相关性很小。在生殖试验中,本品对生育无影响且无致畸性。在非常高的剂量下(按mg/kg计算约为人体最大治疗剂量的150-400倍),胎儿毒性小于母体毒性。本品没有致突变性,也不是主要的致癌物。仅在小鼠体内达到毒性剂量水平时(按mg/kg计算约为人体最大治疗剂量的50-100倍),才能观察到由泌乳素介导的轻度乳腺增生和肿瘤生成。
在麻醉豚鼠的体内模型中,静脉注射给予总剂量为9.87mg/kg(按mg/kg计算约为人体最大治疗剂量的50倍)的氟桂利嗪,结果显示对QTc间期和心电图均无影响。
盐酸氟桂利嗪为选择性钙拮抗剂,可阻滞过量的钙离子跨膜进入细胞内,防止细胞内钙负荷过量,也可防止缺血缺氧时大量钙进入神经元,改善脑微循环及神经元代谢,抑制脑血管痉挛、血小板凝聚及血液粘滞度增高等,此外还有细胞膜稳定作用。本品脂溶性高,易透过血脑屏障。
本品对心脏收缩和传导无影响。
毒理研究
本品的非临床中枢神经系统作用(如;镇静、唾液分泌和共济失调)仅当暴露量远远超过人体的最大暴露量时才观察到,与临床使用的相关性很小。
对本品的安全性进行了一系列综合的非临床研究,包括:单次口服给药的毒性(小鼠、成年及幼年大鼠、豚鼠)、腹膜内(小鼠和大鼠)、皮下(小鼠和大鼠)、静脉(小鼠和大鼠)以及动脉内(大鼠)给药;重复口服给药的毒性(犬12个月和大鼠18个月多剂量的口服毒性)、静脉毒性(犬3个月和大鼠1个月);口服给药的生殖试验测试大鼠的生育和总体繁殖能力;大鼠、兔和出生前、后大鼠的致畸性和胚胎毒性。对本品的致突变性进行了一系列广泛的研究,包括:鼠伤寒沙门氏菌的体外位点和/或基因突变试验、果蝇的伴性隐性致死试验、人体内淋巴细胞的染色体畸变试验、小鼠的体内微核和显性致死试验。利用口服给药后小鼠和大鼠模型的寿命评估本品致癌性。
单次口服给药的毒性试验(小鼠的LD 50约为960-1896mg/kg;大鼠的LD 50约为343-1935mg/kg)结果与人体的最大治疗剂量(对50kg的患者约为0.2mg/kg)相比,本品有很大的安全范围。大鼠和犬重复口服给药的毒性试验结果显示一些临床作用可能与过度的药理作用相关,但都是在远远超过药物治疗剂量时观察到的(按mg/kg计算约为人体最大治疗剂量的400倍),且与临床使用的相关性很小。在生殖试验中,本品对生育无影响且无致畸性。在非常高的剂量下(按mg/kg计算约为人体最大治疗剂量的150-400倍),胎儿毒性小于母体毒性。本品没有致突变性,也不是主要的致癌物。仅在小鼠体内达到毒性剂量水平时(按mg/kg计算约为人体最大治疗剂量的50-100倍),才能观察到由泌乳素介导的轻度乳腺增生和肿瘤生成。
在麻醉豚鼠的体内模型中,静脉注射给予总剂量为9.87mg/kg(按mg/kg计算约为人体最大治疗剂量的50倍)的氟桂利嗪,结果显示对QTc间期和心电图均无影响。
药代动力学
本品吸收良好,口服后2-4小时血药浓度达到峰值,连续服用5-6周达到稳态。
吸收
氟桂利嗪经由胃肠道吸收良好(>80%),口服给药后2-4小时内达到血药浓度峰值。在胃酸降低的情况下(胃pH值升高),其生物利用度会适当下降。
分布
氟桂利嗪与血浆蛋白结合率>99%。本品在健康人体和癫痫患者中均有很大的分布容积,前者接近78L/kg,后者接近207L/kg,说明在品在血管外分布广泛。本品能迅速穿透血脑屏障,在脑中的浓度比在血浆中约高10倍。
代谢
氟桂利嗪在肝中代谢为至少15种代谢物。其主要代谢途径为CYP2D6酶。
消除
氟桂利嗪主要以原形药及其代谢物的形式经胆汁随粪便排出。在给药后的24—48小时内,约有3—5%的剂量以原形药和代谢物的形式从粪便中排出,少于1%的剂量以原形药由尿排出。其终末消除半衰期是高度可变的,在大多数个体中单次给药后的变化范围为5—15小时。一些受试者在一个延长期内(至第30天)可测到本品的血药浓度(>0.5mg/mL),这可能是由于本品在其他组织中的重新分布。
多剂量给药
在每日一次的多剂量给药下,氟桂利嗪的血药浓度约8周后达到稳态,且比同剂量单次给药的浓度高3倍。在5—30mg的范围内,本品的血药浓度与给药剂量成正比。
吸收
氟桂利嗪经由胃肠道吸收良好(>80%),口服给药后2-4小时内达到血药浓度峰值。在胃酸降低的情况下(胃pH值升高),其生物利用度会适当下降。
分布
氟桂利嗪与血浆蛋白结合率>99%。本品在健康人体和癫痫患者中均有很大的分布容积,前者接近78L/kg,后者接近207L/kg,说明在品在血管外分布广泛。本品能迅速穿透血脑屏障,在脑中的浓度比在血浆中约高10倍。
代谢
氟桂利嗪在肝中代谢为至少15种代谢物。其主要代谢途径为CYP2D6酶。
消除
氟桂利嗪主要以原形药及其代谢物的形式经胆汁随粪便排出。在给药后的24—48小时内,约有3—5%的剂量以原形药和代谢物的形式从粪便中排出,少于1%的剂量以原形药由尿排出。其终末消除半衰期是高度可变的,在大多数个体中单次给药后的变化范围为5—15小时。一些受试者在一个延长期内(至第30天)可测到本品的血药浓度(>0.5mg/mL),这可能是由于本品在其他组织中的重新分布。
多剂量给药
在每日一次的多剂量给药下,氟桂利嗪的血药浓度约8周后达到稳态,且比同剂量单次给药的浓度高3倍。在5—30mg的范围内,本品的血药浓度与给药剂量成正比。
贮藏
包装
有效期
执行标准
批准文号
生产企业
核准日期
修订日期
2008年08月01日 2009年06月16日 2010年09月14日 2011年01月11日
$firstVoiceSent
- 来自原声例句