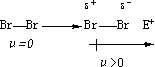分子在外界电场(试剂、溶剂、极性容器)的影响下,键的极性也发生一些改变,这种现象叫极化性。例如:正常情况下Br—Br键无极性,
μ=0,但当外电场E+接近时,由于E+的诱导,引起正负电荷中心分离,出现了键矩
μ:
这种由于外界电场的影响使分子(或共价键)极化而产生的键矩叫做诱导键矩,它与极性共价键的键矩
μ不同,在极性共价键中,
μ是由于成键原子电负性不同引起的,因此是永久性的。而诱导键矩则是在外界电场的影响下产生的,是一种暂时的现象。它随着外界电场的消失而消失,所以叫瞬间偶极。
不同的共价键,对外界电场的影响有不同的感受能力,这种感受能力通常叫做可极化性。共价键的可极化性越大,就愈容易受外界电场的影响而发生极化。键的可极化性与成键电子的流动性有关,亦即与成键原子的电负性及原子半径有关。成键原子的电负性愈大,原子半径愈小,则对外层电子束缚力愈大,电子流动性愈小,共价键的可极化性就小;反之,可极化性就大。
键的可极化性对分子的反应性能起重要作用。例如:
C—X 键的极性:C—F > C—Cl > C—Br > C—I
C—X 键的可极化性:C—I > C—Br > C—Cl > C—F
C—X 键的化学活性:C—I > C—Br > C—Cl > C—F
可见键的可极化性与化学活性有密切关系。